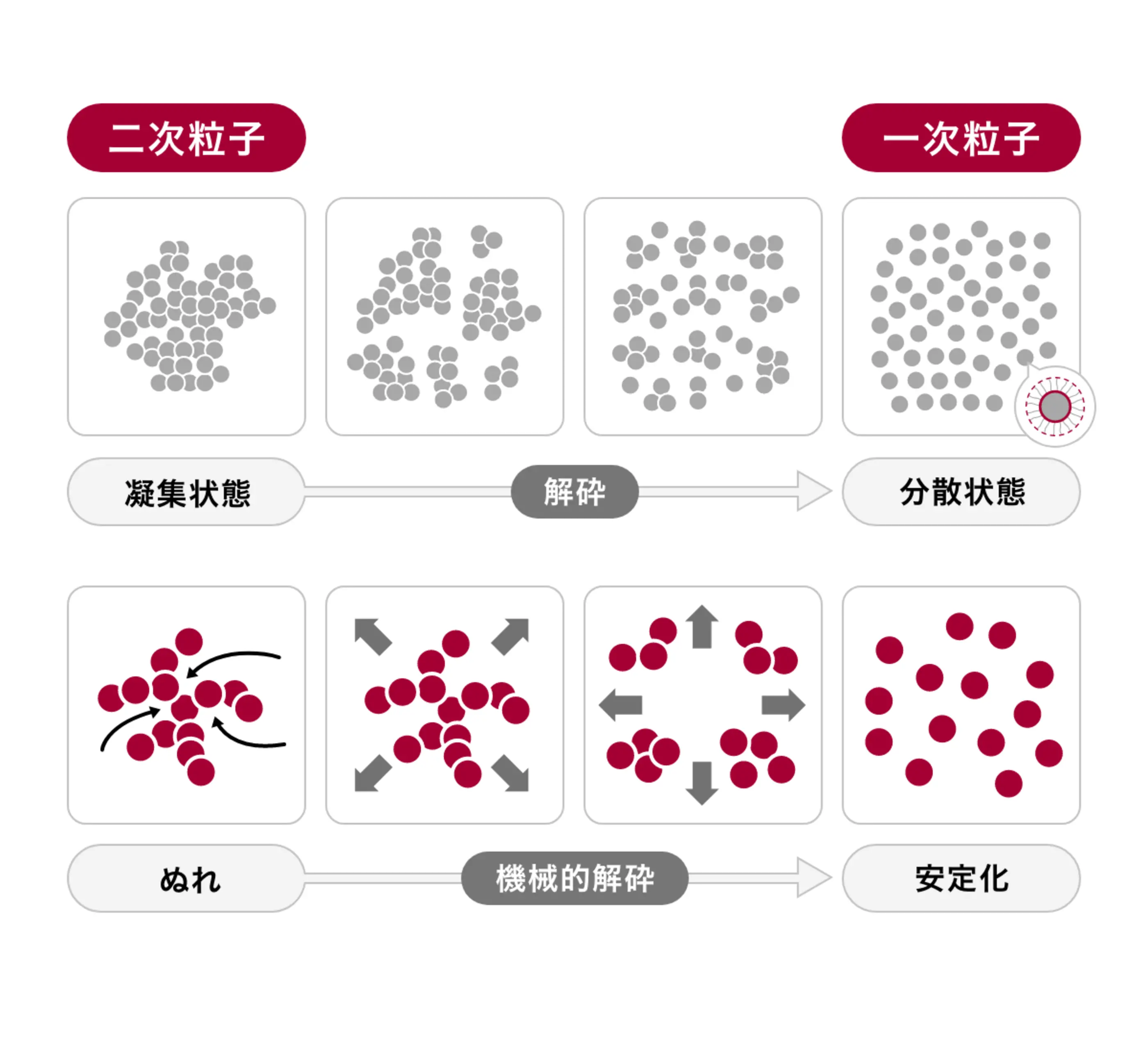
エンドトキシン除去技術とは
基礎知識と代表的な除去方法
April 02, 2026
医薬品や医療機器、再生医療、研究分野などにおいて、エンドトキシンの管理・除去は製品の安全性と品質を左右する重要な課題です。しかし、エンドトキシンは耐熱性・耐薬品性が高く、通常の滅菌処理では十分に対応できないケースも少なくありません。
本記事では、エンドトキシンの基礎知識から、代表的な除去方法、それぞれの特徴について解説します。
エンドトキシンとは
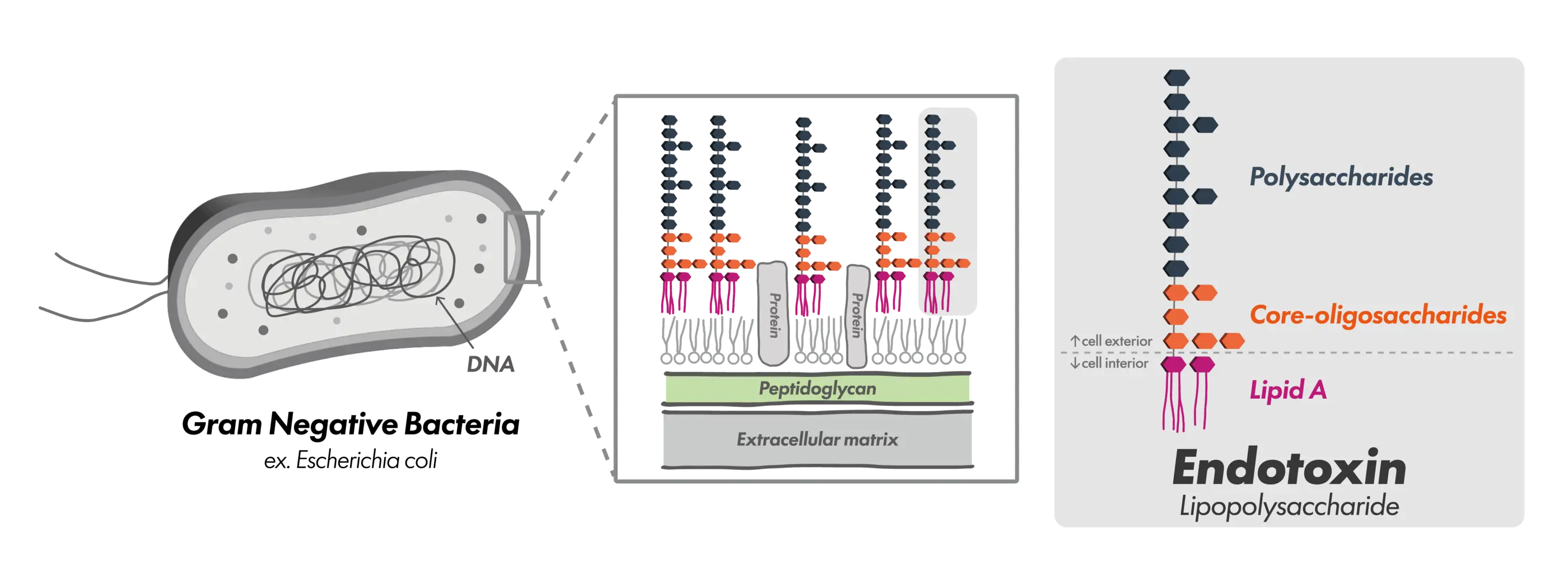
エンドトキシンとは、グラム陰性菌の細胞外膜を構成するリポ多糖(Lipopolysaccharide:LPS)のことで、菌体の死滅・破壊時や、増殖の過程で放出される生理活性物質です。特に脂質部分である「リピドA」がその生理活性の中心となります。
エンドトキシンは環境中に広く存在し、水道水や土壌、空気中など、あらゆる場所に潜んでいます。
エンドトキシンは極めて微量でもヒトに強い発熱反応や炎症反応を引き起こすことが知られており、注射剤や医療機器、再生医療分野などでは厳格な管理が求められています。
また、耐熱性や耐薬品性が高く、通常の滅菌処理では失活しにくいという厄介な性質を持っています。そのため、単なる微生物除去とは異なり、専用のエンドトキシン低減化対策が必要とされます。
エンドトキシン除去の重要性
エンドトキシンが除去されないまま医薬品や医療機器、培養関連製品・細胞治療製品・再生医療製品などに使用された場合、ヒトに重篤な生体反応を引き起こすリスクがあります。
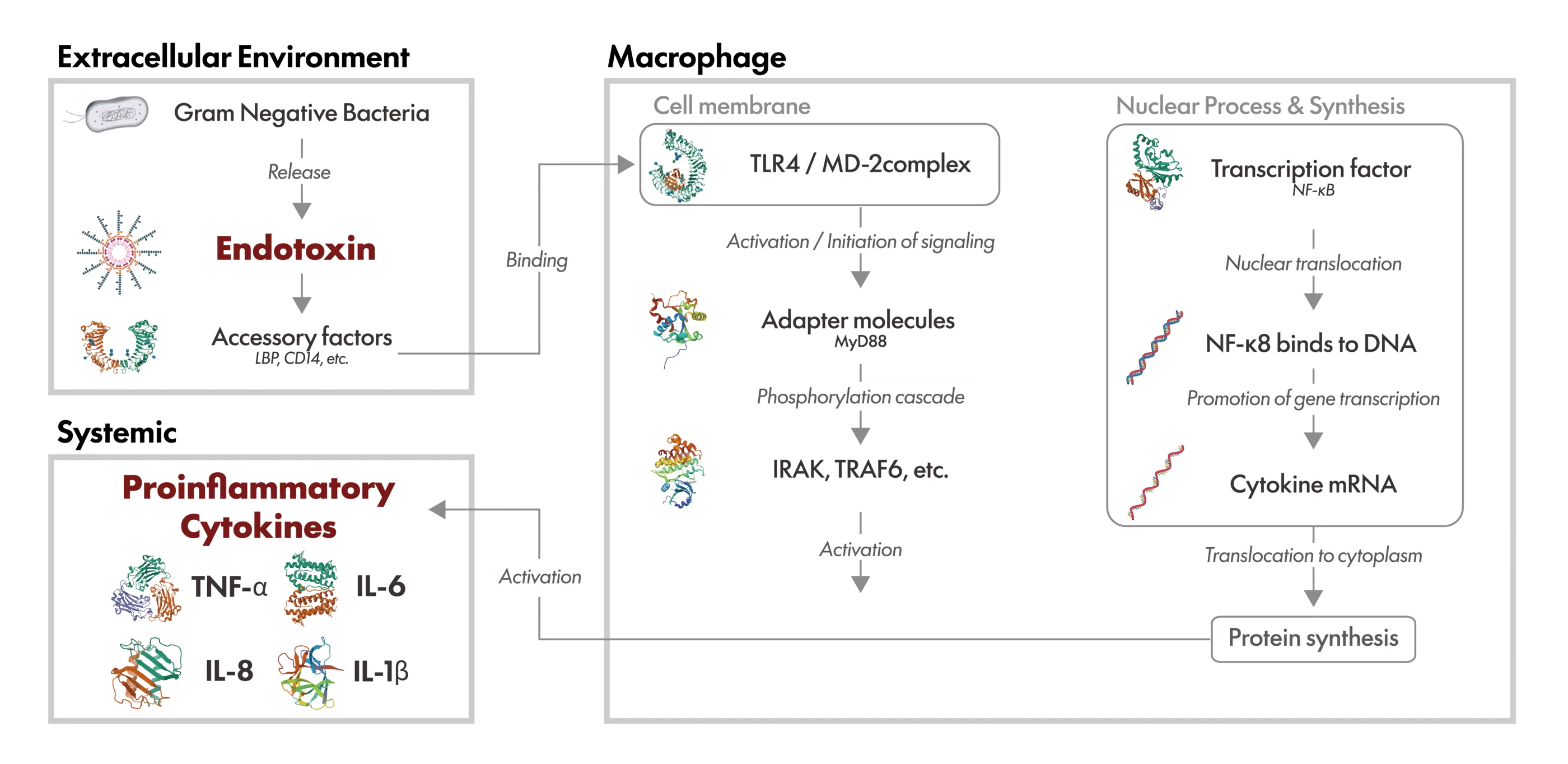
代表的な症状として、発熱、悪寒、炎症反応、血圧低下、重症例では、多臓器不全、敗血症性ショックなどが報告されています。これは、体内の免疫細胞(マクロファージなど)がエンドトキシンを異物として認識し、Toll-like receptor 4(TLR4)を介して細胞内にシグナルを伝え、炎症性サイトカイン(TNF-α・IL-1β・IL-6・IL-8など)の過剰な産生を誘発するためです。
特に注射剤や血液と直接接触する医療機器では、極めて微量のエンドトキシンであっても重大な健康被害につながる可能性があります。
また、エンドトキシンは通常の滅菌処理では完全に失活しにくいため、無菌試験に適合していても、エンドトキシンが残留しており安全性が担保されないケースがあります。このため、製品の品質確保や患者安全の観点から、エンドトキシンを確実に除去する工程の設計と管理が不可欠です。
エンドトキシン管理が必要な分野
エンドトキシン管理は、ヒトの体内に直接または間接的に影響を及ぼす製品を扱う分野で特に重要視されています。
| 分野 | 主な対象例 | リスク・課題 | 管理のポイント |
|---|---|---|---|
| 医薬品 | 注射剤 輸液 透析液 ワクチンなど | 直接血管内に入るため、微量でも発熱・ショック・多臓器不全などの重篤な副作用に直結する。 | 製造用水から最終製品まで、無菌かつパイロジェン(エンドトキシン)フリーであることを厳格に保証する。 |
| 医療機器 | カテーテル インプラント 人工臓器 人工透析回路など | 血液や脳脊髄液に直接接触し、表面の汚染物質が体内に溶出するリスクがある。 | 製品自体の清浄度に加え、洗浄工程のバリデーションや、滅菌包装での汚染防止が必須。 |
| 再生医療 細胞治療 | 細胞加工製品 培地 培養容器など | 製品が「生きた細胞」のため、最終工程での加熱滅菌が不可能。汚染=廃棄または健康被害となる。 | 最終滅菌ができないため、培地や試薬などの「原材料段階」での徹底したエンドトキシン除去が唯一の策。 |
| 研究検査 | 免疫細胞実験 分化誘導実験など | エンドトキシンによる「意図しない細胞の活性化」や細胞死が起き、正しい実験データが得られなくなる。 | 実験結果の妥当性・再現性を確保するため、使用する試薬類のエンドトキシンフリー化が求められる。 |
これらの分野では、単に微生物を除去するだけでは不十分であり、エンドトキシンを確実に低減・管理することが製品の安全性と品質を左右します。
エンドトキシンの管理基準
エンドトキシンの管理が求められる分野において、日本薬局方(JP:Japanese Pharmacopoeia)、米国薬局方(USP:United States Pharmacopeia)により、エンドトキシンの管理基準が定められています。
| 分類 | 対象 | 管理基準値 | 主要引用元 |
|---|---|---|---|
| 医薬品 | 一般注射剤 | 5.0 EU/kg | JP 4.01 / USP <85> |
| 髄腔内投与 | 0.2 EU/kg | JP 4.01 / USP <85> | |
| 医療機器 | 一般(血液接触) | < 20 EU/device | USP <161> |
| 髄液接触 | < 2.15 EU/device | USP <161> | |
| 水・溶媒 | 注射用水 | < 0.25 EU/mL | JP各条 / USP <1231> |
| 透析用水 | < 0.050 EU/mL | ISO / JSDT | |
| 研究用 | 細胞培養(目安) | < 0.01∼0.1 EU/mL | 各社基準 |
エンドトキシンの管理基準を達成するために、エンドトキシンを「分解」して除去する方法や、エンドトキシンと「分離」して除去する方法が用いられています。
エンドトキシンを分解する方法
エンドトキシンを分解(破壊)して除去する方法は、LPS(リポ多糖)の構造を物理的・化学的に変化させて生理活性を失わせるアプローチです。ここでは、加熱や薬剤処理、放射線照射など代表的な手法について、不活性化の仕組みを解説します。(注:日本薬局方や米国薬局方に収載されていない、一般的な手法も含みます)
乾熱処理
エンドトキシンは、脂質A(Lipid A)、コア多糖、O抗原からなるリポ多糖(LPS)構造を持ち、その生理活性(発熱活性)は主に「Lipid A」部分に由来します。
乾熱処理は、250℃×30分以上という高温で加熱(乾熱処理)を行い、熱エネルギーによる酸化分解を利用した手法です。これによりLipid Aのエステル結合や分子内構造が破壊され、立体構造が不可逆的に変化します。その結果、ヒトの免疫受容体(TLR4/MD-2複合体)と結合する能力が失われ、エンドトキシンとしての活性が低下します。
※通常のオートクレーブ(121℃湿熱滅菌)では、この分解反応が起きにくいため、エンドトキシンは不活化されません。
強アルカリ処理
強アルカリ処理は、水酸化ナトリウム(NaOH)などの強アルカリ条件下で、化学的な「ケン化」反応を利用した手法です。アルカリによってLipid Aに含まれるエステル結合が加水分解を受け、脂肪酸側鎖が切断されます。これによりLipid Aの立体構造が変化し、ヒトの免疫受容体(TLR4/MD-2複合体)との結合能が失われるため、エンドトキシンは不活性化されます。また、アルカリは多糖鎖部分も断片化させるため、分子全体が水に溶けやすくなり、その後の洗浄工程(リンス)で物理的に除去しやすくなるという利点もあります。
| NaOH濃度 | 処理温度 | 処理時間 |
|---|---|---|
| 1.0 M | 室温 | 1~2 時間 |
| 0.5 M | 室温 | 4~12 時間 |
| 0.1 M | 室温 | 16 時間以上 |
| 0.5 M + EtOH* | 室温 | 30~60 分 |
*エタノールなどの有機溶媒を併用すると、疎水性の高いLPSへの浸透が早まり、処理時間を短縮できる場合があります。
酸化剤処理
酸化剤処理は、過酸化水素、次亜塩素酸、オゾンなどの強力な酸化剤(特にヒドロキシラジカル・OH を発生させるもの)を用いる手法です。 これらの薬剤は、Lipid Aに含まれる脂肪酸鎖や多糖部分を酸化し、分子内の結合を切断します。その結果、LPSの立体構造が崩壊し、ヒトの免疫受容体(TLR4/MD-2複合体)と結合できなくなるため、生理活性が失われます。
過酸化水素低温ガスプラズマ処理
過酸化水素低温ガスプラズマ処理は、過酸化水素ガスをプラズマ化し、生成した高反応性の活性種(ラジカル)とUV(紫外線)を利用して処理する方法です。 活性種による化学的な「酸化作用」に加え、プラズマ中のイオンによる物理的な「エッチング作用(削り取る作用)」が働きます。これにより、Lipid Aの脂肪酸鎖や多糖構造が分解・除去されます。 ※過酢酸を併用する「過酸化水素/過酢酸プラズマ」では、過酢酸の強力な酸化力が加わることで、より効率的な不活化が期待されます。
電子線・ガンマ線照射
電子線(EB)やガンマ線照射は、高いエネルギーで微生物のDNA/RNAを破壊する「滅菌法」として広く利用されています。しかし、エンドトキシンへの効果は処理条件(水分の有無)によって大きく異なります。
エンドトキシンの活性中心であるLipid Aは、DNAやRNAと比較して放射線に対する耐性が極めて高いため、通常の滅菌線量(25 kGy程度)では乾燥状態のエンドトキシンを十分に不活化できません。 一方、水溶液中では、水の放射線分解によって生じるラジカル(間接作用)がLPSを攻撃するため、比較的低い線量でも分解が進みます。
| 目的 | 状態 | 照射線量の目安 | 効果 |
|---|---|---|---|
| 滅菌 (無菌性保証) | 通常 | 15∼25 kGy | DNA/RNAの破壊により、無菌性保証水準 (SAL10-6)を達成。 ただしエンドトキシンは残存する可能性が高い。 |
| エンドトキシンの分解 | 乾燥 | >100 kGy | 直接作用のみのため、構造破壊には非現実的な高線量(基材劣化を招くレベル)が必要となる。 |
| 水溶液 | 10∼50 kGy | 水の放射線分解で生じるヒドロキシラジカル・OH がLipid Aを酸化分解する(間接作用)。 |
高圧蒸気(オートクレーブ)処理
高圧蒸気処理は、高温の飽和水蒸気を用いる湿熱処理であり、微生物の滅菌(121℃×15~20min)に広く用いられています。しかし、湿熱でエンドトキシンを不活性化するには、121℃×5時間以上、もしくは130℃~140℃×数時間という、標準的な滅菌条件をはるかに超える過酷な条件が必要です。
水分の存在下で十分な熱エネルギーが加わると、多糖部分やLipid Aに含まれる結合が加水分解され、分子構造が変化します。その結果、LPSの立体構造が維持できなくなり、ヒトの免疫受容体(TLR4/MD-2複合体)と結合するために必要な構造が失われます。
しかし、この条件は医薬製品や医薬品やゴム・プラスチック製品にとっても過酷過ぎるため、加水分解や熱変性が起きやすく、エンドトキシン分解方法としては実用的ではありません。
酵素分解
酵素分解は、特定の酵素を用いてエンドトキシンの構成成分を分解し、不活性化する方法です。化学薬剤や高温処理と異なり、酵素分解は比較的温和な条件で作用するため、対象物へのダメージを抑えながら処理できる点が特徴です。ただし、酵素反応は溶液のpHや温度、共存物質の影響を受けやすく、完全に不活化するための反応制御が難しいという課題もあります。
| 酵素 | 標的部位 | 反応 | 結果(構造変化) |
|---|---|---|---|
| Acyloxyacyl Hydrolase (AOAH) | 二次アシル鎖 (脂肪酸) | 脱アシル化 (加水分解) | 6本鎖 → 4本鎖* *ヒト好中球などが持つ防御機構。活性が大幅に低下 |
| Alkaline Phosphatase (ALP) | リン酸基 | 脱リン酸化 (加水分解) | Diphosphoryl → Monophosphoryl* *リン酸基が外れることで受容体への結合能が弱まる |
エンドトキシンと分離する方法
エンドトキシン除去には、化学的・物理的に構造を破壊(不活化)する方法だけでなく、エンドトキシンの構造や性質を維持したまま、物理的に分離・除去する方法も広く用いられています。
蒸留
蒸留は、液体を沸騰・気化させた後に、再凝縮させることで、不純物を分離する古典的な方法です。エンドトキシンは分子量が大きく揮発性を持たないため、水が水蒸気(液体)になる過程で気相へ移行せず、蒸留残渣側に残留します。そのため、凝縮して得られる蒸留液体は、エンドトキシンが含まれにくくなります。主に「注射用水」などの製薬用水や精製水、揮発性化合物の製造工程において用いられています。
超濾過・逆浸透膜
超濾過・逆浸透膜は、膜の細孔径や分子ふるい効果を利用して成分を分離する方法です。水溶液中のエンドトキシンは、単量体として存在するだけでなく、疎水結合により巨大な「会合体(ミセル)」を形成しています。そのため、一定以上の分画分子量を持つ膜を通過できません。その結果、水分子や低分子成分のみが透過し、エンドトキシンは膜の上流側で阻止されます。
| エンドトキシン単量体 | エンドトキシン会合体 | |
|---|---|---|
| 分子量(Da) | 10,000 ~ 20,000 | 300,000 ~ 1,000,000 |
| 構成 | Lipid A + Core多糖 + O抗原 (単分子の状態) | 水溶液中で疎水性部分があつまり、巨大なミセルや小胞を形成 |

| 比較項目 | 超濾過 (Ultrafiltration: UF) | 逆浸透 (Reverse Osmosis: RO) |
|---|---|---|
| 分離原理 | サイズ排除 (ふるい分け効果) | 拡散・溶解 / 排除 (浸透圧差を利用した緻密膜透過) |
| 除去メカニズム | 分子サイズによる物理的阻止 ミセル・モノマーをカット | 分子サイズおよび荷電による完全排除イオン・有機物など全て除去 |
| 適用プロセス | タンパク質製剤の精製など | 製薬用水の製造など |
| 課題・リスク | キレート剤や界面活性剤が存在し、ミセルが崩壊すると、分画分子量の大きい膜では漏洩するリスクがある。 | タンパク質などの高分子医薬品溶液には使用できない。(製品ごと除去してしまうため)。 |
界面活性剤
界面活性剤(Surfactants/Detergents)を用いてエンドトキシンを分離することが出来ます。エンドトキシンの両親媒性(Amphiphilic nature)を利用した手法です。
主に「物理的な相分離」を利用する方法と、「化学的な解離作用」を利用する方法の2つがあります。
曇点抽出法
特定の非イオン性界面活性剤(Triton X-114など)が、温度変化によって「水層」と「界面活性剤層」に分離する性質(曇点:Cloud Point)を利用する手法です。
曇点(約22℃)以上に加温すると、疎水性の高いエンドトキシンは界面活性剤層へ取り込まれ(抽出され)、タンパク質が残る水層と分離されます。
ミセル解離・洗浄法
界面活性剤を用いて、エンドトキシンが形成する巨大な会合体(ミセル)を強制的に単量体へ「解離(Dissociation)」させるアプローチです。これにより、タンパク質とエンドトキシンの結合を引き剥がし、後続の「吸着」や「膜分離」の効率を高めるための前処理として利用されます。
| 比較項目 | 曇点抽出法 (Cloud Point Extraction) | ミセル解離・洗浄法 (Dissociation / Washing) |
|---|---|---|
| 代表的な試薬 | 非イオン性 Triton X-114 | 陰イオン性 ドデシル硫酸ナトリウム、デオキシコール酸 非イオン性 Polysorbate 20/80 |
| 分離原理 | 相分離 温度上昇(>22℃)により二層に分離し、疎水性の高いエンドトキシンを界面活性剤層へ分配 | 単量体化 巨大なエンドトキシンミセルを単量体(10-20kDa)に解離させ、タンパク質との結合を切断 |
| メリット | 操作が簡便 タンパク質の回収率を高く維持できる | タンパク質とエンドトキシンの疎水性結合を物理的に引き剥がすこと可能 装置洗浄に有効 |
| デメリット | ・残留リスク: Triton X-114の完全除去が困難 ・UV干渉: Tritonが280nmに吸収を持つため、タンパク質定量が困難になる ・GMPでの採用例は少ない | ・膜透過リスク: 単量体化するため、UF膜(例えば100 kDa)をすり抜けてしまう ・LER現象: 残留するとLAL試験で偽陰性を引き起こす最大のリスク要因となる |
| 主な適用工程 | 初期精製・研究用 (粗抽出液からのエンドトキシン除去など) | 中間精製・洗浄工程 (アフィニティ吸着の前処理など) |
吸着
吸着法は、エンドトキシン分子が持つ「負電荷」や「疎水性」と、吸着材表面のリガンド(官能基)との相互作用を利用して、対象物から分離する方法です。 加熱や分解処理とは異なり、エンドトキシンの構造そのものを破壊するわけではありません。そのため、タンパク質製剤やバイオ医薬品など、熱や薬品に弱く、性状を保持したまま処理したい対象に適しています。
| 分類 | 吸着原理 |
|---|---|
| アフィニティカラム | 生物学的親和性 ポリミキシンBなどが持つ、Lipid Aへの特異的な結合力を利用 |
| アニオン交換樹脂 | 静電相互作用 負電荷を持つエンドトキシンを、正電荷を持つ樹脂で吸着 |
| デプスフィルター | ゼータ電位(正電荷) 膜表面をカチオン修飾し、電気的な引力で吸着・保持 |
| 合成吸着材 | 特異的相互作用 特定のアミノ酸配列や官能基との親和性を利用 |
吸着法は、「カラム法」や「バッチ法」など、処理量や用途に応じた運用形態が選択できる点も特徴です。
カラム法
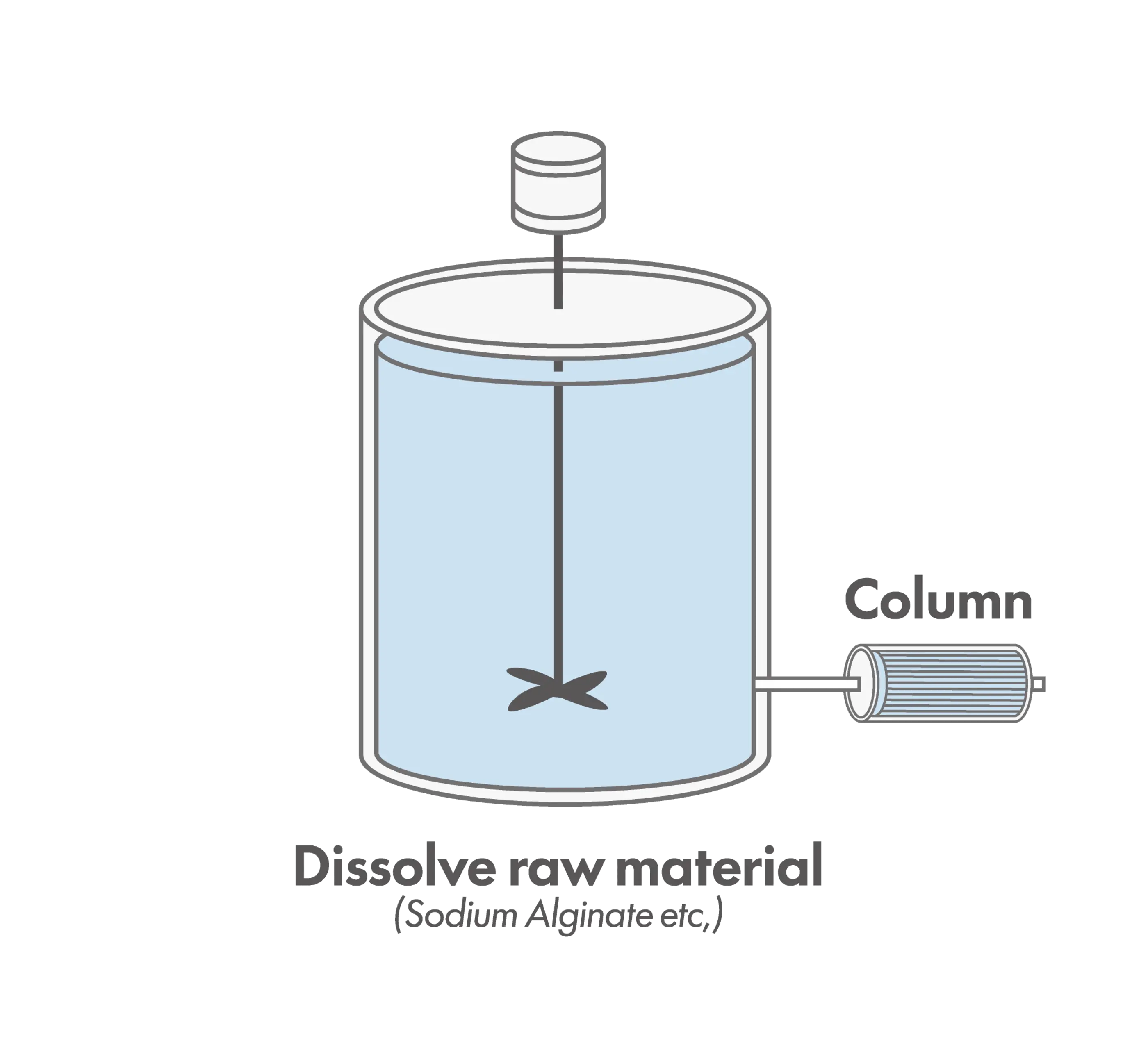
吸着材をカラム(筒状容器)に充填し、液体を連続的に通液してエンドトキシンを除去する方法です。流量や接触時間を制御しやすく、再現性が高いため、製造工程や連続処理に適しています。一方で、装置設計や初期コストが必要になります。
カラム法は吸着原理によって以下のような種類に分けられます。
| 比較項目 | 標準カラム | シリンジカラム | スピンカラム |
|---|---|---|---|
| 操作原理 | 重力 または ポンプ | 手動加圧 | 遠心力 |
| 処理スケール | 数mL ∼ 数百L 製造プロセス向け | 1mL∼ 数mL 簡易処理向け | 10μL∼20mL ラボ・スクリーニング向け |
| 接触時間 | 流速を調整し、十分な結合時間を確保できる。 | 手の押し加減でバラつく。ゆっくり押す必要がある。 | 遠心力と樹脂密度に依存。一瞬で抜けると吸着しない。 |
| 主な用途 | 最終製品の製造 プロセス開発 大量サンプルの精製 | 現場での簡易処理 装置がない環境での処理 | 多数検体のスクリーニング 小スケールの実験 貴重な微量サンプルの処理 |
バッチ法
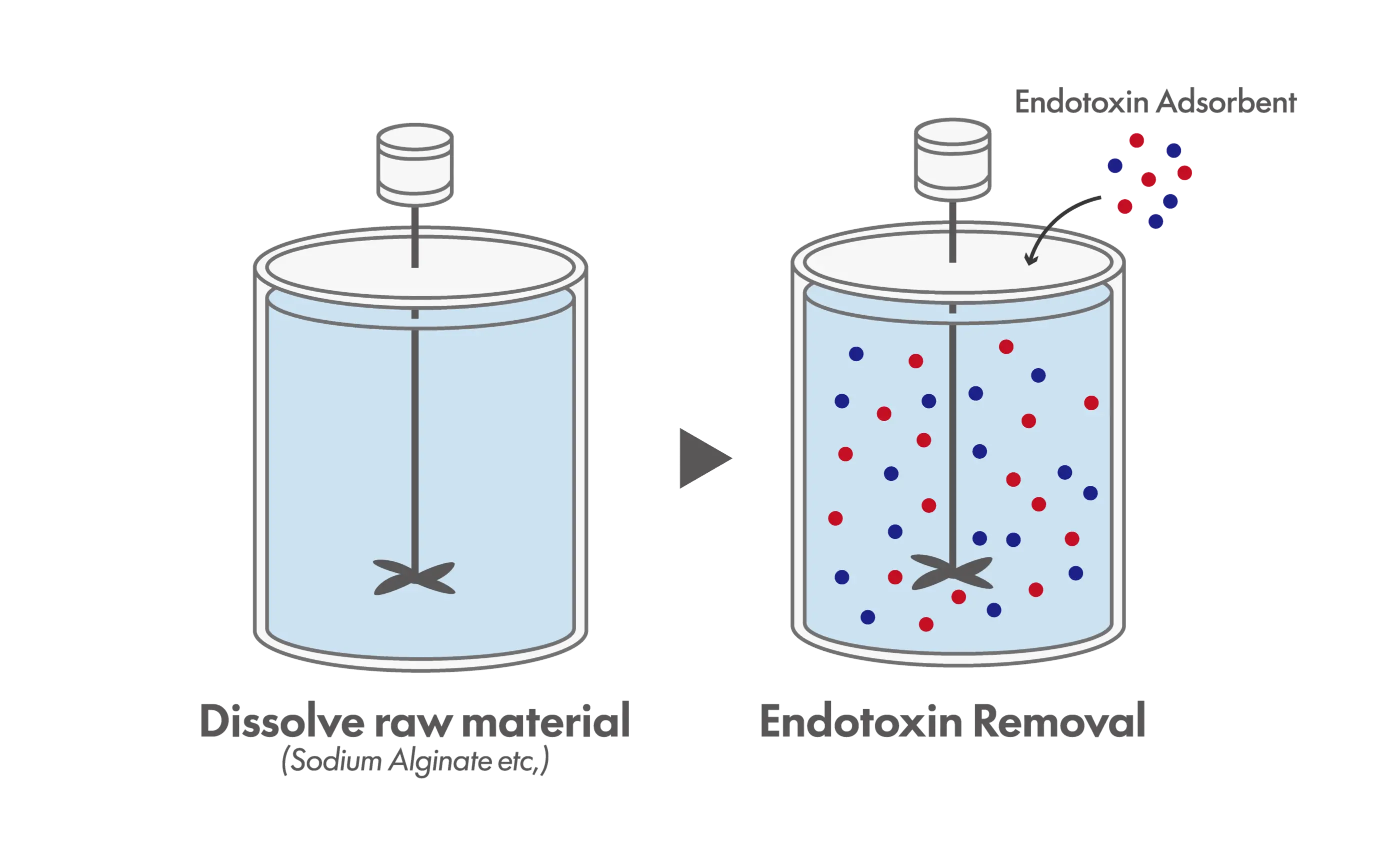
吸着材(ビーズや樹脂)を処理液に直接投入し、一定時間撹拌(インキュベーション)してエンドトキシンを吸着させた後、遠心分離やろ過で吸着材を取り除く方法です。 カラム法と比較して理論的な除去効率は劣る場合がありますが、カラムに詰められない高粘度溶液や、スラリー状のサンプルでも処理できる点が特徴です。近年では、操作が簡便な「磁気ビーズ」を用いたバッチ処理も普及しています。
ナガセケムテックスの除去技術
従来のカラム法や一般的な吸着材には、アルギン酸ナトリウムやキサンタンガムといった「高粘度素材」を通液しようとすると目詰まりを起こす、あるいは圧力で吸着材やカラムが劣化してしまうという課題がありました。
ナガセケムテックスは、これらの課題を解決するために独自の「エンドトキシン除去技術」を確立しました。
独自の吸着材(高選択性・高吸着容量)
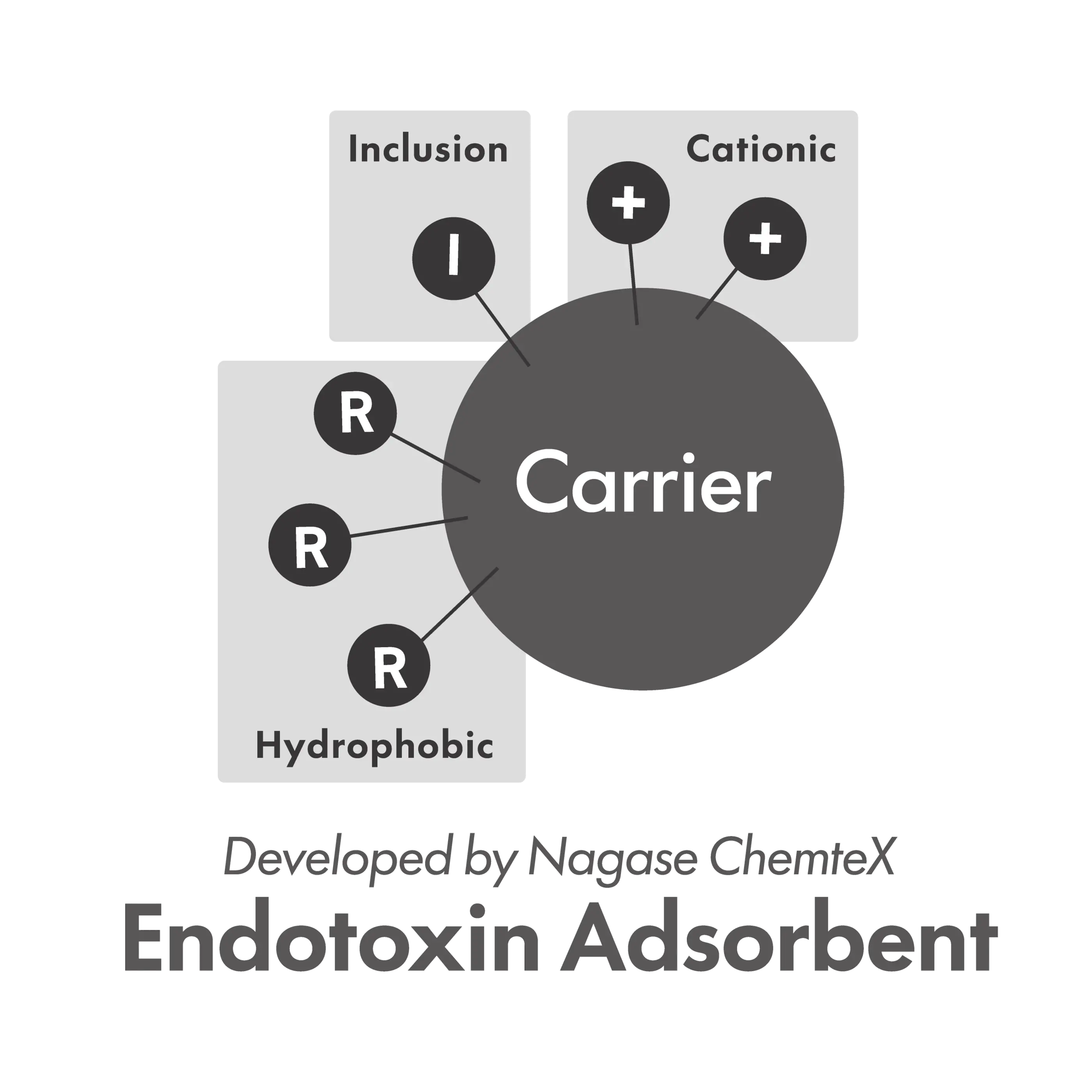
ナガセケムテックスのエンドトキシン吸着材は、熊本大学との共同で開発しました。従来のエンドトキシン吸着材よりもエンドトキシンのみを選択的に吸着できるように担体・リガンドを設計しています。
エンドトキシンの吸着容量も高く、初期エンドトキシン値が高い素材からも、効率的にエンドトキシンを除去することが可能です。
この技術を応用し、フェーズや用途に合わせた3つの形態でソリューションを提供しています。
エンドトキシン除去カラム(研究・試験用)
実験室レベルでの少量サンプルの精製には、カートリッジ型カラム「NEA-1000R」が推奨されます。タンパク質などの有用成分を損なわず、エンドトキシンのみを除去する高い選択性が特徴です。
- 高い回収率(高選択性)
BSA(ウシ血清アルブミン)やγ-グロブリンなどのタンパク質溶液において、エンドトキシン除去率99%以上を達成。同時に、タンパク質回収率も95%以上を維持しており、貴重なサンプルのロスを最小限に抑えます。
- 簡便な操作(Ready-to-use)
製品はEOG滅菌(エチレンオキサイドガス滅菌)済みの個包装で提供されます。シリンジやペリスタポンプに接続し、注射用水などで洗浄するだけですぐに使用可能です。特別な準備や複雑なセットアップは必要ありません。
- 幅広い適用範囲
タンパク質溶液だけでなく、培地、核酸、多糖類(プルランなど)など、多様なサンプルの処理に適しています。
| Sample | Isoelectric Point (pI) | Before Treatment | After Treatment | Removal of Endotoxin Rate | Protein Recovery Rate |
|---|---|---|---|---|---|
| BSA | 4.9 | 30 EU/mL | 0.1 EU/mL | ≧99% | ≧98% |
| γ-globulin | 7.4 | 41 EU/mL | 0.5 EU/mL | ≧99% | ≧99% |
| Cytochrome C | 10.6 | 27 EU/mL | 0.1 EU/mL | ≧99% | ≧96% |
低エンドトキシンバイオマテリアル「Arcofeliz®」
再生医療や医療機器の開発において、アルギン酸ナトリウムやキサンタンガムといった「天然高分子」は、生体適合性の高さから注目されている素材です。しかし、これらの素材は天然由来であるがゆえに「エンドトキシンなどの不純物が多い」、かつ「粘度が高く精製が困難」という大きな課題を抱えていました。
ナガセケムテックスの「Arcofeliz®(アルコフェリス)」シリーズは、独自の除去技術によってこの課題を解決した、高純度・低エンドトキシンバイオマテリアルです。
ナガセケムテックスが保有する独自の「エンドトキシン除去技術」を用いて製造されています。これにより、素材本来の粘度や物性を損なうことなく、医療用途に耐えうるレベルまでエンドトキシンを低減化することに成功しました。
製品ラインナップ
再生医療の足場材(スキャフォールド)、止血材、癒着防止材、DDS基材などの用途に合わせて、複数のラインナップを取り揃えています。
- アルギン酸ナトリウム(Sodium Alginate)
海藻由来の多糖類。
細胞のカプセル化や創傷被覆材などに適しています。
ナガセケムテックス独自の「エンドトキシン除去技術」は、素材本来の物性を損なわずに低エンドトキシン化が可能なので、幅広いラインナップがあります。
・M/G比率(M/G≧1.5, M/G≦0.8, M/G≒1.0)
・粘度(1~1,200mPa・s)
- キサンタンガム(Xanthan Gum)
Xanthomonas campestris(グラム陰性菌)由来の多糖類。
高い増粘性を持ち、医薬品添加剤や機能性ゲルの原料として利用されます。
グラム陰性菌由来のため、含まれているエンドトキシン量が多く、低エンドトキシン化することが困難です。ナガセケムテックスでは、高粘度を維持しつつ、低エンドトキシン化することが可能です。
- ゼラチン(Gelatin)
動物由来のタンパク質。
細胞培養基材やインプラント材として広く使用されています。
人獣共通感染症のリスクがあり、低エンドトキシンゼラチンの共有は不安定になる場合があります。ナガセケムテックスでは、原料Lotに影響されにくく、低エンドトキシンゼラチンを安定供給することが可能です。
- その他(Others)
その他にもラインナップを揃えています。
詳しくは、お問い合わせください。
受託サービス:エンドトキシン除去検討・加工
お客さまが保有する素材をお預かりし、エンドトキシン除去条件の検討を行うサービスです。 数mLの検討段階から、数L規模へのスケールアップまで対応しており、プロセス実装をサポートします。
新しいバイオ医薬品や再生医療など製品の開発において、原材料のエンドトキシン除去は避けて通れない課題です。しかし、自社で最適な除去条件を見つけ出し、さらに製造スケールまで引き上げるには、多大なリソースとノウハウが必要となります。
ナガセケムテックスでは、お客さまの大切な素材をお預かりし、エンドトキシン除去の「条件検討」から「受託加工」までを引き受ける受託サービスを提供しています。
高粘度素材やタンパク質など、数多くの素材を取り扱ってきたナガセケムテックスの知見を活かし、お客さまの素材に最適な「洗浄・除去・回収」のプロセスを提案・構築します。
ラボレベルの少量試験から、プラントでの量産化まで対応可能ですので、まずはお気軽にご相談ください。
【参考文献】
Tsuji, K., et al. (1978). Applied and Environmental Microbiology, 36(5), 710-714.}Csako, G., et al. (1983). Applied and Environmental Microbiology, 45(4), 1342-1350.
Ludwig, J. D., & Avis, K. E. (1985). Journal of Parenteral Science and Technology, 39(6), 258-261.
Munford, R. S., et al. (2009). The Journal of Immunology, 182(10), 5901-5908.
Bates, J. M., et al. (2007). Cell Host & Microbe, 2(6), 371-382.
Aida, Y., & Pabst, M. J. (1990). Journal of Immunological Methods, 132(2), 191-195.
Petsch, D., & Anspach, F. B. (2000). Journal of Biotechnology, 76(2-3), 97-119.
Anspach, F. B. (2001). Journal of Chromatography A, 921(1), 31-46.
Guo, W., et al. (1990). Biomedical Chromatography, 4(2), 67-73.
Hirayama, C., et al. (1994). Journal of Chromatography A, 676(2), 267-275.
- 【薬機法(旧薬事法)に関する重要なお知らせ】
- 本技術の位置づけ:本記事で紹介している製品および技術は、医薬品や医療機器の製造プロセス、または研究開発において使用される「原料」や「処理技術」です。最終製品(医薬品など)の有効性や安全性を保証するものではありません。
- Arcofeliz®について:Arcofeliz®シリーズは、医薬品添加剤や医療機器原材料としての使用を想定した「素材」です。これ単体が疾病の診断、治療、予防を目的とした医薬品ではありません。
- 品質規格:「低エンドトキシン」などの表現は、各製品の規格値に基づく物理化学的な特性を示したものであり、臨床的な効果を標榜するものではありません。
関連商品
お気軽に
ご連絡ください。
右記のフォームにお問い合わせ内容をご入力いただき、個人情報の取り扱いに同意の上「送信する」ボタンを押してください。