アルギン酸ナトリウムのエンドトキシン対策
低エンドトキシン化の限界と解決法
April 02, 2026
アルギン酸ナトリウムは、生体適合性やゲル化能に優れた多糖類として、再生医療や細胞培養、医療機器分野で広く利用されています。一方で、原料や製造工程に由来するエンドトキシンの混入が課題となる場合があり、とくに生体に直接関与する用途では、低エンドトキシン化が不可欠です。
本記事では、アルギン酸ナトリウムとエンドトキシンの関係、低エンドトキシン化が難しい理由、一般的な対策方法について解説します。

アルギン酸ナトリウムとは
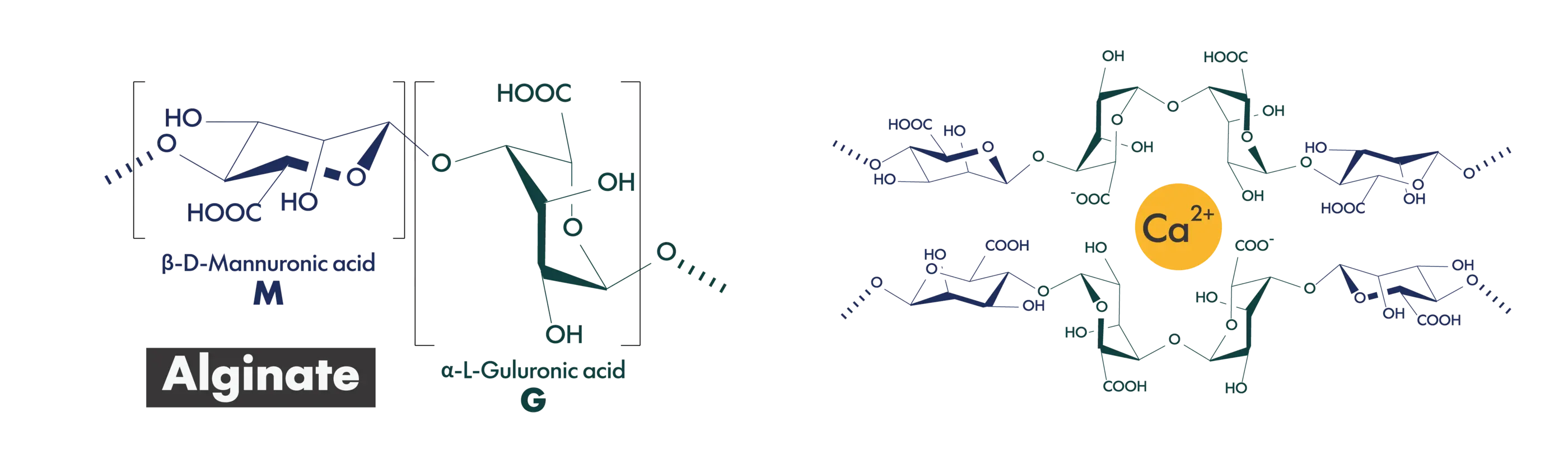
アルギン酸ナトリウムは、コンブやワカメなどの褐藻類に含まれる多糖類であるアルギン酸をナトリウム塩として精製した高分子材料です。主にマンヌロン酸(M)とグルロン酸(G)から構成され、水に溶解すると高い粘性を示します。
また、カルシウムなどの二価金属イオンと反応することでゲル化する特性を持ち、増粘剤、安定剤、ゲル化剤として食品、医薬品、化粧品など幅広い分野で利用されています。近年では、生体適合性の高さから、医薬品、医療機器、再生医療、細胞治療における細胞培養足場材料や細胞内包カプセル化材料としての重要性が急速に高まっています。
アルギン酸ナトリウムの細胞への効果
アルギン酸ナトリウムは、細胞毒性が極めて低く、穏やかな条件でゲル化する性質を持つことから、再生医療や組織工学における「3次元培養の足場材料(スキャフォールド)」として広く利用されています。カルシウムイオンと反応して形成されるハイドロゲルは、生体内の細胞外基質(ECM)に類似した環境を提供します。この柔軟なゲルの中で、細胞は酸素や栄養素をスムーズに受け取りながら、本来の機能を維持して増殖・分化することが可能です。特に、ES細胞やiPS細胞、間葉系幹細胞(MSC)を用いた研究では、細胞をカプセル化することで物理的な保護と適切な微小環境を与え、スフェロイド形成やオルガノイド構築を促進する効果が期待されています。
| 細胞 | 目的・効果 | アルギン酸の役割と成果 |
|---|---|---|
| ヒトES細胞 hESCs | 大量培養 未分化維持 | 【物理的保護】 カプセルが保護壁となり、バイオリアクターのせん断力から細胞を保護。未分化能を維持したまま効率的に細胞増殖。 |
| 間葉系幹細胞 MSCs | 骨再生 分化誘導 | 【分化足場】 RGDペプチド修飾ゲル内で、効率的に骨芽細胞へ分化しミネラル沈着を確認。ゲルの硬さが分化効率に影響する。 |
| がん細胞 Cancer Cells | 薬剤評価 スフェロイド形成 | 【生体模倣】 キトサンとの複合ゲルで、実際の腫瘍に近い球状塊(スフェロイド)を形成。平面培養より抗がん剤抵抗性が高く、生体に近い正確なスクリーニングが可能。 |
| 神経細胞 Neural Cells | 神経再生 | 【成長方向制御】 チューブ状のアルギン酸ゲルにより、トンネル(チャネル)の方向に沿って、一直線に成長。 |
| 軟骨細胞 Chondrocytes | 表現型維持 脱分化抑制 | 【脱分化の防止】 平面培養で起きる繊維芽細胞様への変化(脱分化)を抑制。8ヶ月以上軟骨特有の基質産生を維持することを証明。 |
| 膵島細胞 Pancreatic Islets | 糖尿病治療 免疫隔離 | 【免疫バリア】 酸素や栄養は通すが免疫細胞は通さない「半透膜」として機能。移植後、免疫抑制剤なしで血糖値の正常化に成功。 |
アルギン酸ナトリウムのM/G比率と細胞への効果
アルギン酸ナトリウムの、G(グルロン酸)とM(マンヌロン酸)の比率(M/G比)が変わると、形成されるゲルの「物理的性質(硬さ・弾力)」が劇的に変化し、それが細胞の挙動に直接的な影響を与えます。
| M/G比率 | 対象細胞 | 研究内容 |
|---|---|---|
| G Rich (M/G ≦ 0.8) | 膵島モデル細胞:βTC3 Islet model cells : βTC3 | 【構造安定性の確保】 |
| M Rich (M/G ≧ 1.5) | 膵島モデル細胞:βTC3 Islet model cells : βTC3 | 【物質透過性と細胞増殖】 物質透過性が良いため、細胞増殖・代謝活性が高くなる。 |
| Standard (M/G ≒ 1.0) | 軟骨細胞 Chondrocytes | M Rich, G Richと比較して、良好な生存率と表現型の保存性を示した。SOX9、COL2、aggrecanなどの軟骨特異的遺伝子の発現が増加。 |
低エンドトキシンアルギン酸ナトリウムとは
低エンドトキシンアルギン酸ナトリウムとは、原料由来や製造工程中に混入するエンドトキシンを極力低減したアルギン酸ナトリウムを指します。
食品などの一般用途では問題とならないレベルの微量なエンドトキシン量であっても、再生医療や細胞培養、医療機器など生体に直接関与する用途では、重大なリスクとなります。微量のエンドトキシンが細胞の炎症反応を誘発したり、分化誘導の阻害要因となったりするためです。したがって、医薬品、医療機器、再生医療、細胞治療用途においては、「低エンドトキシン化」されたアルギン酸ナトリウムを選択することが、重要となります。
アルギン酸ナトリウムに含まれるエンドトキシン
アルギン酸ナトリウムにエンドトキシンが含まれる主な要因は、原料が褐藻類などの天然由来である点にあります。海洋環境には多くのグラム陰性菌が存在しており、これらの菌由来のエンドトキシンが原藻に付着・共存した状態で原料に持ち込まれます。
さらに、アルギン酸の抽出・精製工程では、微生物の死滅に伴ってエンドトキシンが放出されやすく、粘性の高い多糖構造に取り込まれやすいという特性があります。このため、通常の洗浄や濾過などの精製工程だけではエンドトキシンが残留しやすく、低エンドトキシン化には特別な工程設計が必要です。
低エンドトキシンアルギン酸ナトリウムの用途
低エンドトキシンアルギン酸ナトリウムは、細胞活性に影響を与えることが知られています。報告されている細胞活性への例を紹介します。
| 対象細胞 | 主な影響 | 内容 |
|---|---|---|
| ヒト間葉系幹細胞 hMSCs | 骨分化の阻害 | エンドトキシンの存在により、TLR4受容体を介してIL-6やIL-8などの炎症性サイトカイン分泌が増加。これにより、骨形成の指標であるALP活性や石灰化が著しく阻害。 |
| 膵島細胞 Pancreatic Islets | 繊維化 | ポリフェノール、エンドトキシン、タンパク質などで汚染されていると、移植部位で炎症が起き、アルギン酸ナトリウムカプセルが膜(繊維)で覆われて機能しなくなる。 |
| マクロファージ Macrophages | 激しい炎症反応 | 微量の不純物(エンドトキシン、ペプチドグリカンやフラジェリン)がTLR(Toll様受容体)を刺激し、炎症性サイトカイン放出を誘導。 |
| リンパ球 / 単球 Lymphocytes / Monocytes | 細胞分裂の誘発(Mitogenic) | エンドトキシンやタンパク質の汚染が免疫細胞を異常に刺激・増殖させ、強い拒絶反応を引き起こす。 |
このように、低エンドトキシンアルギン酸ナトリウムは、細胞や生体組織と直接関わる用途を中心に、安全性や機能性、評価の再現性を確保するために不可欠な材料となっています。
アルギン酸ナトリウムを低エンドトキシン化する際の課題
アルギン酸ナトリウムは、生体適合性やゲル化能といった有用な特性を持つ一方で、エンドトキシン除去を目的とした一般的な処理条件に対して性質が変化しやすい高分子材料です。特に、加熱や化学処理はエンドトキシン低減に有効である反面、アルギン酸ナトリウム本来の物性に影響を与えてしまいます。ここでは、アルギン酸ナトリウムを低エンドトキシン化する際に生じる代表的な課題について解説します。
| 処理方法 | エンドトキシン 不活化の原理 | アルギン酸への影響・課題 |
|---|---|---|
| 乾熱処理 | 加熱(250℃など) による熱分解 | 【耐熱性不足】 エンドトキシン分解温度より低い60~100℃でアルギン酸が分解・炭化するため、適用不可。 |
| 酸化剤処理 | 酸化反応による 不活化 | 【分子鎖切断】 フリーラジカルがアルギン酸の糖鎖を切断し、粘度・分子量が減少。 |
| アルカリ処理 | pH13以上での 加水分解 | 【耐アルカリ性】 エンドトキシン分解よりも先に、pH10以上でアルギン酸ナトリウムの「β-脱離反応」が進行し、分解・変性する。 |
| 膜処理 (UF/RO膜) | 分子サイズによる ふるい分け | 【分離困難】 ①高粘度による目詰まり・ゲル層形成。 ②エンドトキシンのミセル化により、アルギン酸ナトリウムと分子量サイズが重複し分離できない。 |
| 吸着処理 | 電荷・疎水性 による吸着 | 【非特異的吸着・高粘度】 ①アルギン酸も「負電荷」を持つため、エンドトキシンと一緒に吸着され、回収率が低下する。 ②高粘度のため、吸着材内部への拡散が遅く、十分なエンドトキシン除去効果が見込めない。 |
乾熱処理による課題
ガラス器具などの滅菌で一般的に用いられる「乾熱処理」は、アルギン酸ナトリウムも分解してしまうため、乾熱処理は適用できません。
アルギン酸ナトリウムは、マンヌロン酸(M)とグルロン酸(G)が直鎖状に結合した多糖類です。加熱により糖鎖の「グリコシド結合」が加水分解や熱分解を起こし、分子鎖が切断されます。その結果、本来の粘度が著しく低下し、ゲル化能が失われてしまいます。
- エンドトキシンの分解条件
250℃で30分、または180℃で3~4時間の加熱が必要
- アルギン酸ナトリウムの耐熱限界
60~100℃程度の加熱から分解開始
酸化剤処理による課題
過酸化水素などの酸化剤を用いることで、エンドトキシンを分解し、不活性化することができます。しかし、酸化剤処理を行うと、発生したフリーラジカル(ヒドロキシラジカル・OHなど)がアルギン酸ナトリウムの糖鎖(グリコシド結合)を切断してしまうため、分子量低下、低粘度化に繋がります。
そのため、粘度や強度を維持する必要がある用途(細胞培養や組織工学など)において、酸化剤処理はアルギン酸ナトリウムのエンドトキシン低減化方法として、現実的な選択肢ではありません。
アルカリ処理による課題
エンドトキシンは、0.1M~1.0M NaOHなどのアルカリ条件(pH13以上)で、エンドトキシンに含まれるLipid Aの脂肪鎖のエステル結合が加水分解(ケン化)され、エンドトキシンとしての活性が失われます。一方、アルギン酸ナトリウムは、pH10以上のアルカリ条件下にすると、β-脱離反応が進行しやすくなり、糖鎖(グリコシド結合)が切断され、分子量低下が起こります。また、強アルカリ条件ではM/G比率や配置が変化する可能性があり、カルシウム架橋によるゲル形成能や機械的特性が変わります。
- エンドトキシンの分解条件(pH13以上)
0.1M~1.0M NaOHなどの強アルカリ条件下で、リピドA(毒性中心)のエステル結合が加水分解(ケン化)され、毒性が失われる
- アルギン酸のナトリウムの分解条件(pH10以上)
pH10を超えると、アルギン酸特有の分解反応である「β-脱離反応」が進行します。これによりグリコシド結合が切断され、分子量が低下
限外ろ過(UF膜)・逆浸透膜(RO膜)による課題
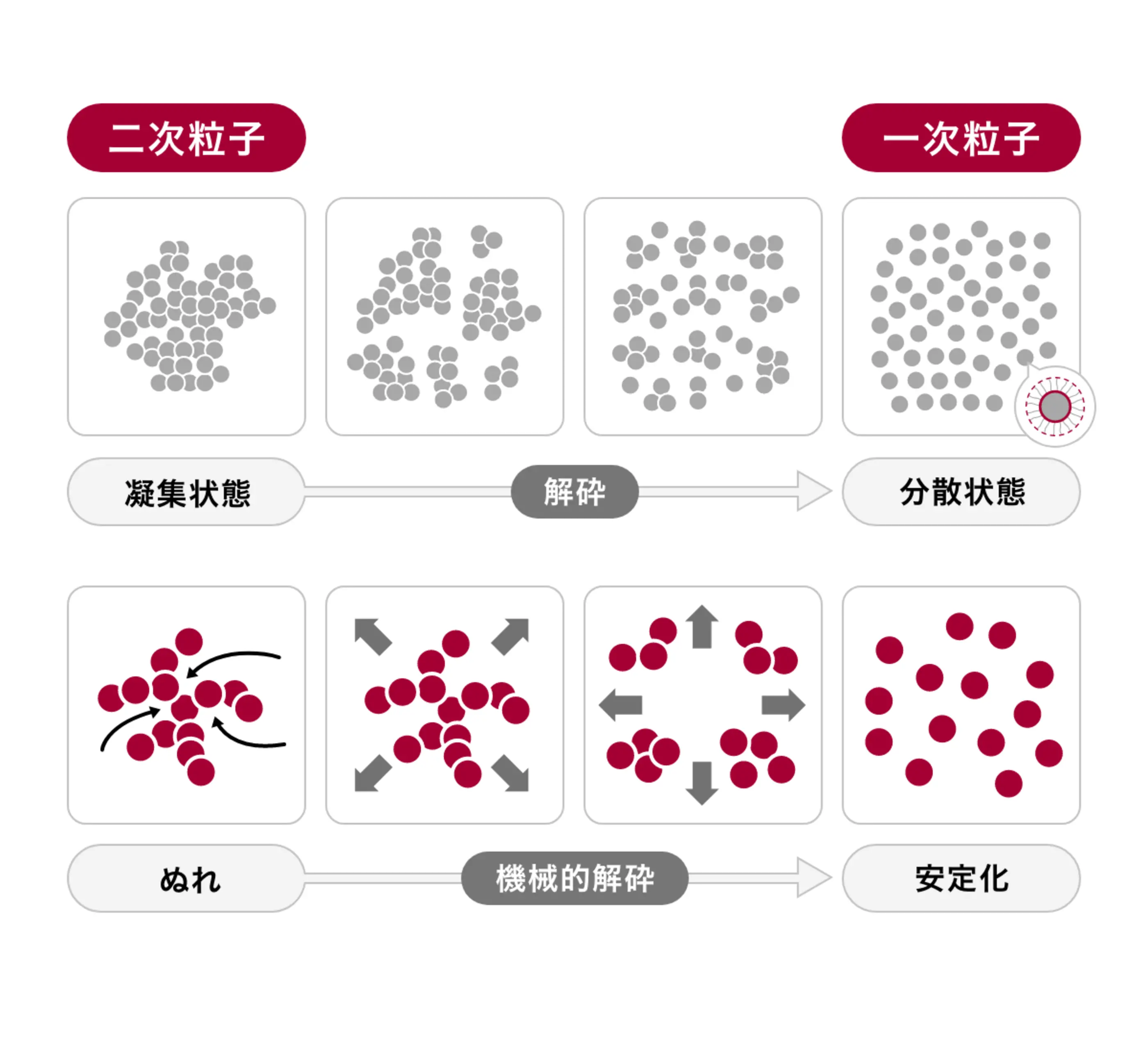
水溶液中のエンドトキシンは、単量体として存在するだけでなく、疎水結合により巨大な「会合体(ミセル)」を形成しています。そのため、一定以上の分画分子量を持つ膜を通過できません。その結果、水分子や低分子成分のみが透過し、エンドトキシンは膜の上流側で阻止されます。
エンドトキシンの分子量(単量体・ミセル)を利用して、限外ろ過(UF膜)・逆浸透膜(RO膜)を用いて、エンドトキシンを低減化することが出来ます。
熱や薬品を使わないので、アルギン酸ナトリウムの低エンドトキシン処理に活用できる可能性がありますが、「高粘度」「分子サイズ」が課題となります。
- 高粘度による操作性悪化
アルギン酸ナトリウムは、水溶液中で高い粘性を示します。この粘性は、巨大な分子量と分子鎖同士の絡み合いに由来します。高い粘度により、流動性が低下するため、濾過時の圧力損失が大きくなります。その結果、フィルターが目詰まりを起こしたり、膜表面にゲル層が形成されたりして、処理が困難になります。
- 分子サイズの重複
分子量により、エンドトキシンを膜分離できますが、エンドトキシンとアルギン酸ナトリウムの分子量が重なってしまう可能性があります。
- エンドトキシンの分子量
単量体:1~2万 Da
ミセル:100万 Da以上
- アルギン酸ナトリウムの分子量
数千~数百万 Da
ミセル化したエンドトキシンは、アルギン酸ナトリウムと同様に「100万Da以上」の巨大分子として振る舞うため、分画分子量による分離ができません。
一方で、膜の孔径を小さくしてエンドトキシンを阻止しようとすると、アルギン酸自体も膜を通過できなくなり、回収率が著しく低下します。
そのため、アルギン酸ナトリウムの低エンドトキシン処理に、限外ろ過(UF膜)・逆浸透膜(RO膜)は適していません。
吸着処理の課題
エンドトキシン除去では、電荷や疎水性相互作用を利用した吸着法が有効な手段となる場合があります。しかし、アルギン酸ナトリウムは、多数のカルボキシル基(-COOH)を持つ、酸性の高分子多糖であり、分子全体が強い負電荷を帯びています。
- 負電荷による「非特異的吸着」と回収率の低下
正電荷をもつ吸着材を用いることで、負電荷のエンドトキシンを吸着することが出来ます。アルギン酸ナトリウムも負電荷をもつため、正電荷をもつ吸着材に吸着されてしまう可能性があります。その結果、アルギン酸ナトリウムも吸着除去され、収率も低下します。
- 高粘度による「吸着効率の低下」
吸着材が機能するためには、対象物質が吸着材の細孔の奥深くまで入り込む(拡散する)必要があります。しかし、アルギン酸ナトリウム溶液は粘度が高いため、内部への物質移動が制限されます。吸着材表面への拡散がスムーズに行われず、吸着平衡に達するまでに長時間を要したり、十分な除去性能が発揮されなかったりと、処理が不安定になる要因となります。
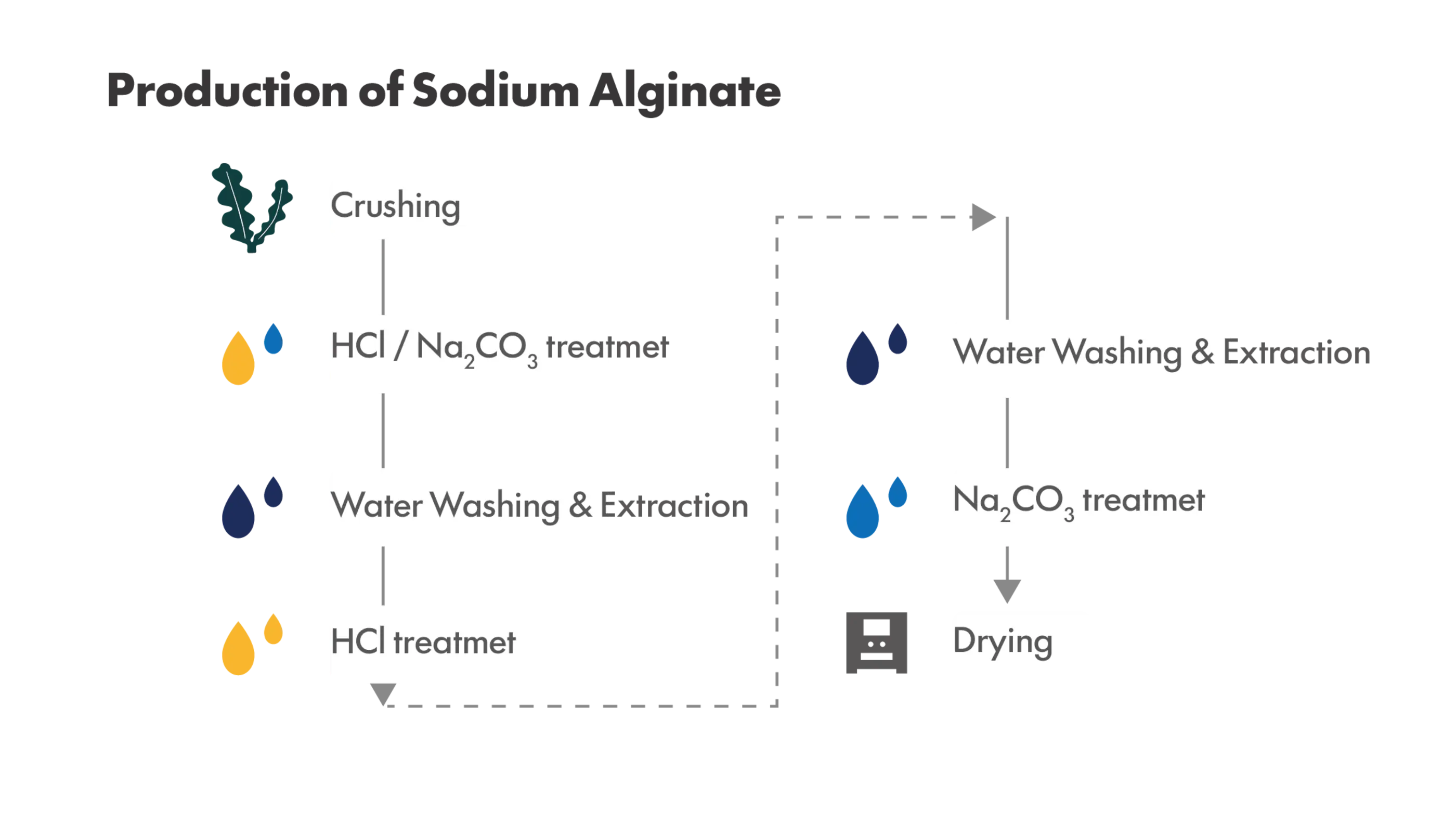
アルギン酸ナトリウムを低エンドトキシン化する方法
アルギン酸ナトリウムの低エンドトキシン化には、原料処理や精製工程の工夫が用いられてきました。しかし、アルギン酸ナトリウムは酸性の高分子多糖であり、エンドトキシンと物性や挙動が近いことから、一般的な処理方法では十分な低減が困難です。特に、高粘度のアルギン酸ナトリウムの低エンドトキシン化は非常に困難です。以下に、アルギン酸ナトリウムの低エンドトキシン化する方法とその特徴を示します。
| 手法 | 原理 | 備考 |
|---|---|---|
| 限外ろ過 (UF) | 分離膜で分離 | 高粘度のため希釈が必要 エンドトキシンのミセル化により分離困難な場合がある |
| 界面活性剤 + 限外ろ過(UF) | ミセル破壊 + 分離膜で分離 | 界面活性剤の除去工程が必要 |
| 吸着法 (活性炭) | 疎水性相互作用で吸着 | アルギン酸ナトリウムも非特異的に吸着されやすく、回収率が悪い |
| 吸着法 (ポリミキシンB修飾樹脂) | 特異的相互作用で吸着 | 非常に高価 リガンド脱離のリスク管理が必要 |
限外ろ過(UF)
アルギン酸ナトリウムのような高分子は膜を通過できず、エンドトキシンや低分子の不純物だけが膜を通過して排出することが出来ます。一方で、アルギン酸ナトリウムが高粘性のため、膜がすぐに目詰まりを起こす問題もあります。限外ろ過を行う場合、膜が目詰まりしないようにアルギン酸ナトリウムの濃度を薄くする必要があります。
界面活性剤 + 限外ろ過(UF)
エンドトキシンの会合(ミセル)状態によっては、限外ろ過できない場合があります。
その際、界面活性剤を用いてエンドトキシンの会合状態を崩すことで、限外ろ過によるエンドトキシン低減化が出来るようになります。一方で、高粘度のアルギン酸ナトリウムは処理できない課題は解消されず、使用した界面活性剤を除去する工程が必要になります。
吸着法(活性炭)
エンドトキシンの毒性部分(リピドA)は、脂質でできており疎水性を持っています。活性炭は疎水性の物質を吸着する力が強いため、アルギン酸溶液を活性炭に通すことで、エンドトキシンの脂質部分を吸着・除去します。一方で、アルギン酸ナトリウムも吸着されてしまい、収率(歩留まり)が下がる傾向があります。エンドトキシンの吸着量も多くないので、含まれているエンドトキシンの量が多いと処理できない課題があります。
吸着法(ポリミキシンB修飾樹脂)
「ポリミキシンB」という抗生物質は、エンドトキシンのリピドA部分と特異的に結合する性質を持っています。このポリミキシンBを固定化したビーズや膜にアルギン酸ナトリウム溶液を通すと、アルギン酸ナトリウムは吸着せず、エンドトキシンだけが吸着させることが出来ます。しかし、ポリミキシンBが非常に高価であるため、実験室レベルや高付加価値な医療用製品に用途が限られます。
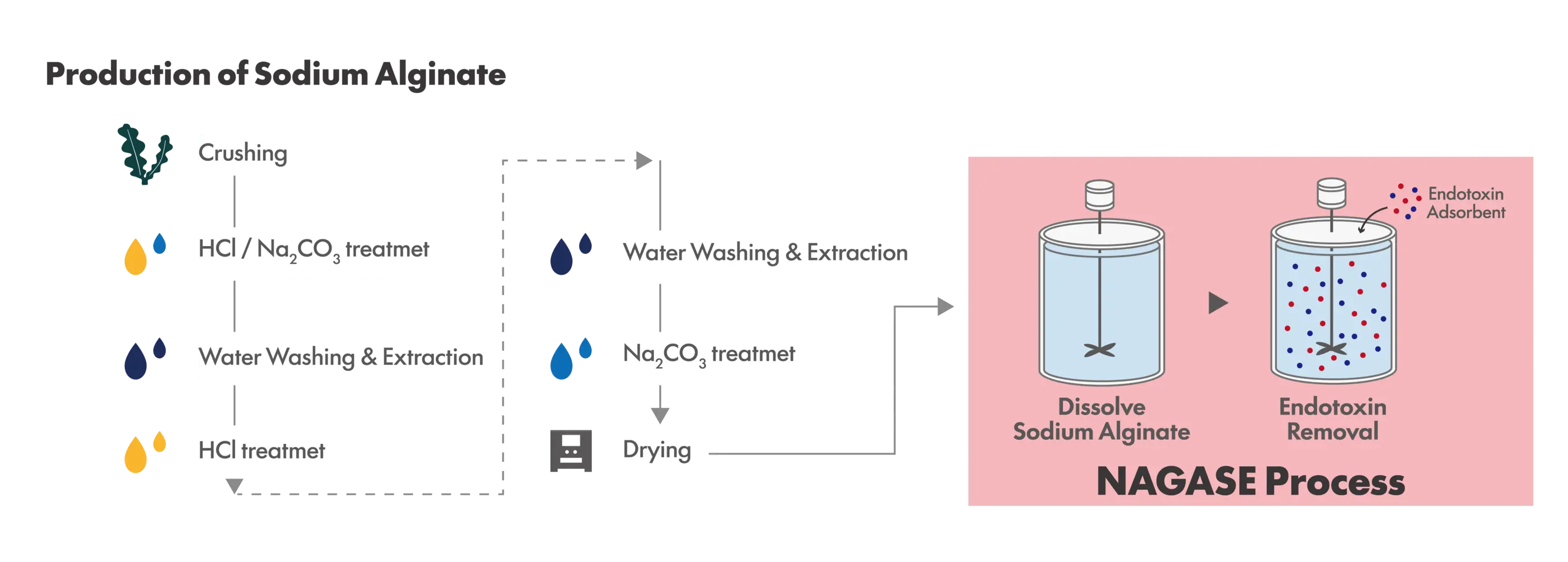
ナガセケムテックスの低エンドトキシンアルギン酸ナトリウム
ナガセケムテックスでは、ポリミキシンBを使用せず、エンドトキシンを特異的に吸着できるエンドトキシン吸着材を設計しました。吸着法により、エンドトキシンを効率的に除去できます。原料のLotや組成依存が少なく、複数グレードの低エンドトキシンアルギン酸ナトリウムをラインアップしており、Arcofeli® ALシリーズとして提案しています。
特長
・低エンドトキシン管理 < 30EU/g
・幅広い粘度グレード(1~1,200 mPa・s)
・3タイプのM/G比(M/G≧1.5, M/G≦0.8, M/G≒1.0)
・低エンドトキシン処理専用設備の設計
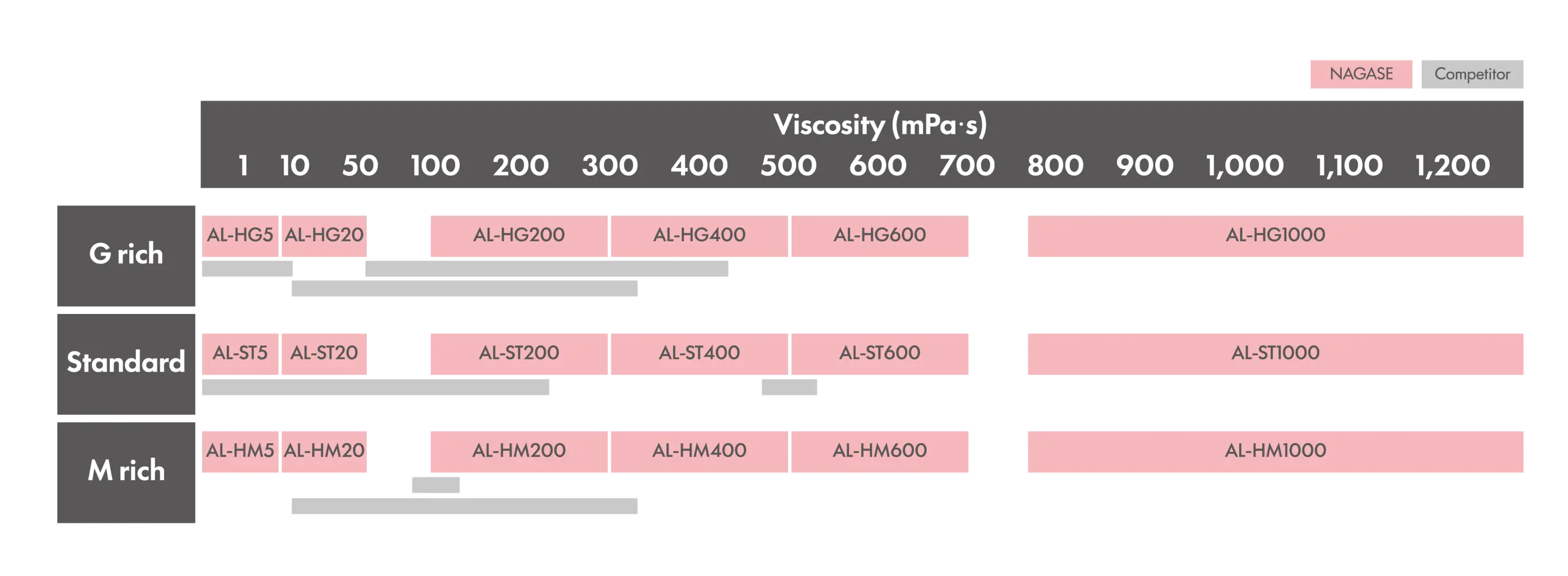
ナガセケムテックスの低エンドトキシンアルギン酸ナトリウムは、エンドトキシン含有量が低く、非常に高純度です。
| メーカー | エンドトキシン値 |
|---|---|
| ナガセケムテックス | <10EU/g(高純度グレード) |
| <30EU/g | |
| 他社品A | <50EU/g * |
| 他社品B | <100EU/g * |
*公開情報を元に比較しています。
低エンドトキシンアルギン酸ナトリウムについてご興味のある方は、まずはお気軽にご相談ください。
【参考文献】
Siti-Ismail, N., et al. (2008). Biomaterials, 29(29), 3946-3952.
Wang, L., et al. (2010). Biomaterials, 31(7), 1848-1857.
Kievit, F. M., et al. (2010). Biomaterials, 31(14), 3903-3913.
Prang, P., et al. (2006). Biomaterials, 27(19), 3560-3569.
Häuselmann, H. J., et al. (1994). Journal of Cell Science, 107(Pt 1), 17-27.
Lim, F., & Sun, A. M. (1980). Science, 210(4472), 908-910.
Stabler, C., et al. (2001). Biomaterials, 22(10), 1301-1310.
Lee, B. B., et al. (2012). Journal of Biomaterials Science, Polymer Edition, 23(1-4), 185-199.
Klöck, G., et al. (1997). Biomaterials, 18(10), 707-713.
Dusseault, J., et al. (2006). Journal of Biomedical Materials Research Part A, 76(2), 243-251.
Paredes Juarez, G. A., et al. (2014). Journal of Controlled Release, 172(3), 983-992.
Paredes Juarez, G. A., et al. (2010). Journal of Biomedical Materials Research Part B, 93(2), 333-340.
Holme, H. K., et al. (2008). Carbohydrate Polymers, 73(4), 656-664.
- 【薬機法(旧薬事法)に関する重要なお知らせ】
- 本技術の位置づけ:本記事で紹介している製品および技術は、医薬品や医療機器の製造プロセス、または研究開発において使用される「原料」や「処理技術」です。最終製品(医薬品など)の有効性や安全性を保証するものではありません。
- Arcofeliz®について:Arcofeliz®シリーズは、医薬品添加剤や医療機器原材料としての使用を想定した「素材」です。これ単体が疾病の診断、治療、予防を目的とした医薬品ではありません。
- 品質規格:「低エンドトキシン」などの表現は、各製品の規格値に基づく物理化学的な特性を示したものであり、臨床的な効果を標榜するものではありません。
関連商品
お気軽に
ご連絡ください。
右記のフォームにお問い合わせ内容をご入力いただき、個人情報の取り扱いに同意の上「送信する」ボタンを押してください。